2021年《中国心血管疾病健康与疾病报告》中指出,心血管疾病是中国居民主要疾病死亡中的首位死因[1]。动脉粥样硬化是心血管疾病中的主要病理过程[2-5]。乳杆菌有益于人体健康,在增强免疫力、促进消化吸收、预防治疗腹泻等方面发挥作用[6-11]。鼠李糖乳杆菌(LGG)与嗜酸乳杆菌(LA)属于乳杆菌属,是公认的益生菌菌株,在维持菌群平衡、促进胃肠道健康、抑制有害菌增殖方面发挥作用[12]。有研究结果显示,LGG与LA具有抑制动脉粥样硬化的作用[13-15]。本研究经过文献调研筛选了两株益生菌LGG与LA,探讨其联合干预对动脉粥样硬化的影响是否优于单独菌株干预,以期为临床动脉粥样硬化的预防和治疗提供更多的策略。
1 材料与方法 1.1菌株鉴定与培养实验菌株LGG购于北纳生物科技有限公司(编号为BNCC 134266),LA购于广东省微生物菌种保藏中心(编号为GDMCC 1.208)。
1.1.1 革兰染色、测序将购买的菌株活化,通过革兰染色、送样测序(16s rRNA v3-v4区)等方式鉴定菌株。
1.1.2 菌株培养与灌胃菌液配制将购买的菌株活化,通过革兰染色、送样测序(16s rRNA v3-v4区)等方式鉴定菌株。
1.1.3 菌株耐酸性质检测菌株均在37 ℃恒温厌氧箱中培养。4 ℃条件下,以8 000 r/min离心5 min收集3代菌株,用无菌磷酸盐缓冲溶液(PBS)重悬洗涤2次,采用平板计数法获得菌体浓度为25×1011 CFU /L的灌胃菌悬液。
1.1.4 菌株耐胆盐性质检测人胃的pH值一般在2.5~3.0之间,食物经过胃消化时间为1~2 h[16-17],因此实验中设置pH为1.0、2.0、3.0共3个梯度,耐酸性培养时间设置为3 h。收集3代菌株将其接种到pH为1.0、2.0、3.0的培养液中,培养3 h后进行平板稀释涂布,36~48 h后计数。每组重复3次。
1.2 动物模型与分组菌株是否耐胆盐判断标准是其在3 g/L胆盐浓度条件下的存活率[18],食物经肠道消化时间为2~3 h,因此设置培养时间为4 h。收集3代菌株,分别接种到胆盐浓度为2、3、4 g/L的培养液中,培养4 h后进行平板稀释涂布,36~48 h后计数。每组重复3次。实验选用8周龄的55只雄性APOE基因敲除(APOE-/-)小鼠与11只雄性C57BL/6J小鼠,小鼠购自唯尚立德生物科技有限公司。所有小鼠被随机分为空白对照组(C57BL/6J小鼠,A组)、实验对照组(APOE-/-小鼠,B组)、LGG组(APOE-/-小鼠,C组)、LA组(APOE-/-小鼠,D组)和混合物组(APOE-/-小鼠,E组),每组11只。5组小鼠的初始平均体质量为21 g左右。小鼠饲养在25 ℃、严格12 h光/暗循环的条件下。C57BL/6J小鼠喂养普通生长繁殖饲料,APOE-/-小鼠喂养含质量分数0.150 0脂肪和0.002 5胆固醇的高脂肪高胆固醇饲料。
适应性饲养1周后,每天上午开始灌胃实验。A组与B组小鼠灌胃无菌PBS,C组灌胃LGG,D组灌胃LA,E组灌胃LGG与LA,均灌胃200 μL。连续灌胃12周,处死小鼠。采用摘眼球取血,并将血清分离保存。同时收集并保存主动脉、肝脏、肠等组织待测。
1.3 主动脉动脉粥样硬化病理学分析主动脉固定在40 g/L多聚甲醛中,6~8 h后,转移到150 g/L的蔗糖溶液里,处理过夜。转移到300 g/L的蔗糖溶液里,处理过夜。进行OCT包埋,主动脉根部横截面冷冻切片。主动脉主体直接进行油红O染色,主动脉根部横截面冷冻切片后采用油红O染液进行染色,显微镜下观察拍照并使用Image J软件对结果进行量化分析。
1.4 小鼠血清血脂含量检测小鼠眼球取血,按照检测试剂盒说明书对小鼠血清总胆固醇(TC)、高密度脂蛋白(HDL)和低密度脂蛋白(LDL)水平进行检测。
1.5 RT-qPCR检测主动脉炎症因子与肝脏胆固醇转运分子的表达水平利用TRIzol试剂按照说明书分别提取主动脉与肝脏RNA。以GAPDH作为内参照。按照试剂盒说明进行反转录和RT-qPCR。PCR所用引物及其序列见表 1。
| 表 1 RT-qPCR扩增引物及其序列 |
|
|
利用GraphPad prism统计软件进行数据分析。计量资料使用x±s表示,多组比较采用单因素方差分析(one-way ANOVA检验)进行,采用LSD法进行组间两两比较。以P < 0.05为差异具有统计学意义。
2 结果 2.1 菌株鉴定革兰染色结果显示,这两种菌株均被染为紫色,为革兰阳性菌,且呈短棒状,符合乳杆菌的形态结构(图 1a、c)。使用DNASTAR软件将得到的测序结果序列与标准菌株序列、对照序列进行同源性比对,结果显示,LGG菌株与LGG标准序列几乎完全重合,LA菌株与LA标准序列几乎完全重合,确定LGG和LA菌株(图 1b、d)。
 |
| a:LGG革兰染色镜检图,100倍;b:LGG菌株16s rRNA测序结果部分对比结果图,LGG strain.seq为LGG标准菌株序列,RNA Seq-1.seq为所购LGG测序序列,Ref 1.seq与Ref 2.seq为对照序列;c:LA革兰染色镜检图,100倍;d:LA菌株16s rRNA测序结果部分对比结果图,LA strain.seq为LA标准菌株序列,RNA Seq-1.seq为所购LA测序序列,Ref 1.seq与Ref 2.seq为对照序列。 图 1 LGG与LA菌株鉴定图 |
酸性条件pH=1.0时,LGG与LA菌株的存活率为0;酸性条件pH=2.0时,LGG的存活率为(78.10±2.98)%,LA的存活率为(92.80±3.22)%;酸性条件pH=3.0时,LGG的存活率为(50.77±0.45)%,LA的存活率为(43.67±4.86)%。见图 2a、b。
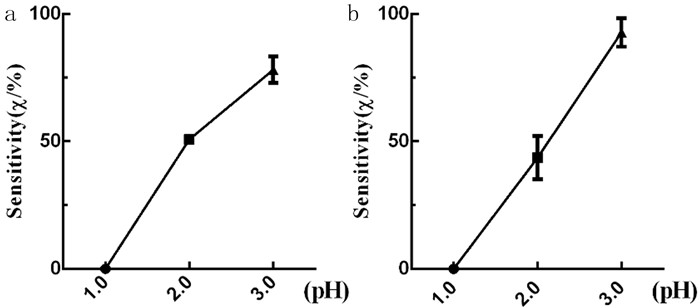 |
| a: LGG菌株在不同pH值下的耐酸性存活率;b:LA菌株在不同pH值下的耐酸性存活率。 图 2 菌株在不同pH值条件下的耐酸性存活率 |
在胆盐浓度为2 g/L时,LGG菌株存活率为(94.63±0.87)%,LA菌株的存活率为(77.30±3.33)%;在胆盐浓度为3 g/L时,LGG的存活率为(60.63±2.42)%,LA的存活率为(64.03±2.54)%;在胆盐浓度为4 g/L时,LGG的存活率为(43.57±0.91)%,LA的存活率为(37.23±1.68)%。见图 3a、b。
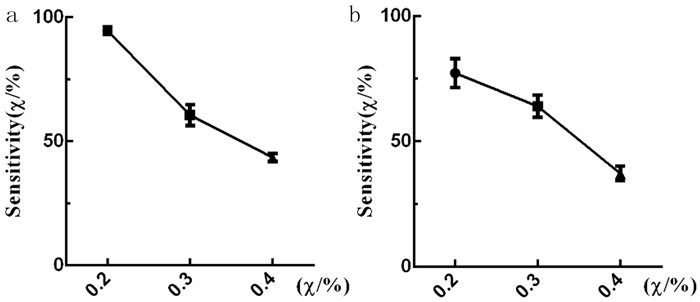 |
| a:LGG菌株在不同胆盐浓度下的耐胆盐性存活率;b:LA菌株在不同胆盐浓度下的耐胆盐性存活率。 图 3 菌株在不同胆盐浓度下的耐胆盐性存活率 |
根据前期文献结果[13, 19-20],确定给药途径为灌胃给药,给药剂量为5×108CFU。实验过程中对小鼠体质量进行记录,结果显示,20周龄的5组小鼠体质量差异有统计学意义(F=11.73,P < 0.05)。两两比较结果显示,A组小鼠体质量低于实验组各组小鼠(tLSD=3.370 ~ 6.379,P < 0.05),各实验组APOE-/-小鼠之间体质量并无差异(P>0.05)。各组小鼠的肝脏质量、心脏质量之间无明显差异(P>0.05)。见表 2。灌胃12周后处死小鼠,选取主动脉根部横截面与主体内膜面进行油红O染色,同时对主动脉根部横截面和主体内膜面斑块面积占比进行测定。结果显示,5组小鼠的主动脉主体内膜面与根部横截面斑块面积相比较差异有统计学意义(F=26.29、86.45,P < 0.001)。A组小鼠的主动脉未出现斑块病变(图 4A、5A)。两两比较结果显示,B组小鼠的主动脉主体内膜面(图 4B)和根部横截面(图 5B)斑块面积与A组小鼠相比明显增大(tLSD=9.471、16.44,P < 0.05)。益生菌干预后小鼠主动脉主体内膜面(图 4C~F)和根部横截面(图 5C~E, 图 6)斑块积累情况得到明显改善,斑块面积都明显减少。两两比较结果显示,E组斑块面积小于C组、D组(tLSD=2.642~4.307,P < 0.05)。
| 表 2 各组小鼠脏器质量比较(n=11,m/g,x±s) |
|
|
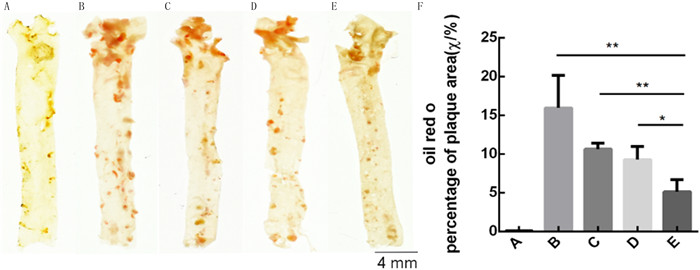 |
| A:空白对照组;B:实验对照组;C:LGG组;D:LA组;E:混合物组。F:各组小鼠主动脉主体内膜面斑块面积占比比较。与E组相比,*P<0.05,**P < 0.01。 图 4 小鼠主动脉主体内膜面斑块油红O染色图 |
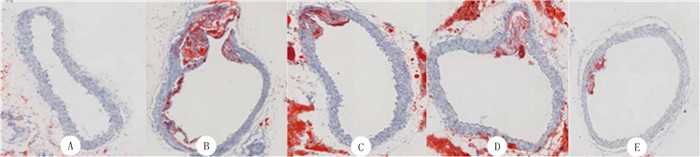 |
| A:空白对照组;B:实验对照组;C:LGG组;D:LA组;E:混合物组。油红O染色。 图 5 小鼠主动脉根部横截面斑块油红O染色图 |
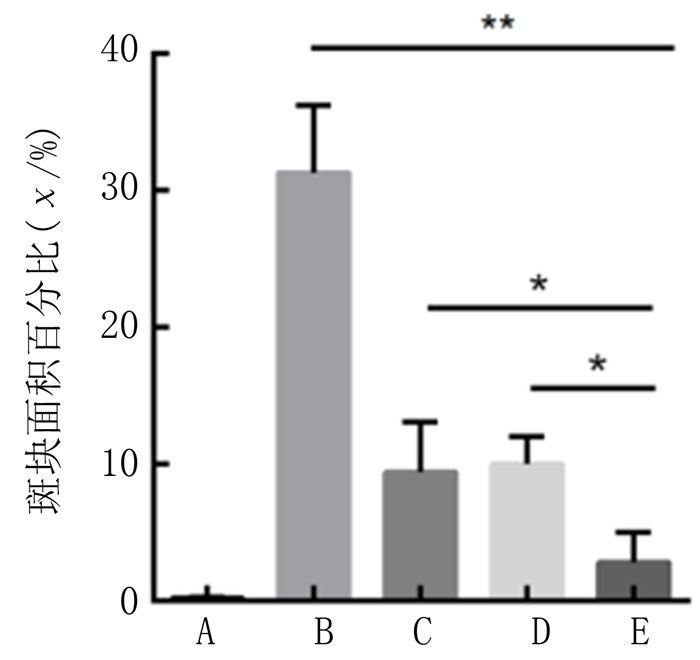 |
| 与E组相比,*P < 0.05,**P < 0.01。 图 6 各组小鼠主动脉根部横截面斑块面积占比比较 |
5组小鼠肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)表达水平比较差异有统计学意义(F=56.68、23.41,P < 0.001)。两两比较结果显示,与A组小鼠相比,B组小鼠的TNF-α与IL-6表达水平显著升高(tLSD=13.310、7.746,P < 0.01);采用益生菌联合干预后,TNF-α、IL-6的表达水平显著降低。两两比较结果显示,E组的TNF-α与IL-6表达水平低于C组、D组(tLSD=3.918~5.533,P < 0.05)。见图 7。
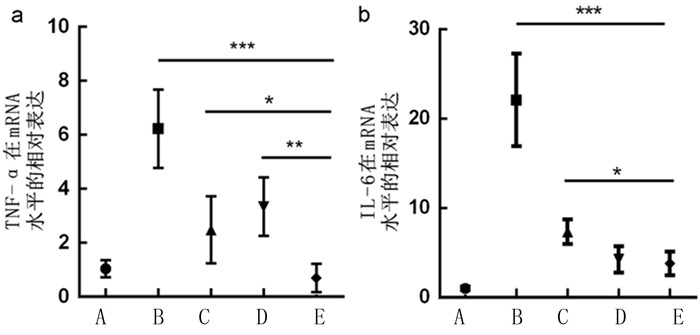 |
| a:小鼠主动脉TNF-α的表达水平;b:小鼠主动脉IL-6的表达水平。A:空白对照组;B:实验对照组;C:LGG组;D:LA组;E:混合物组。与E组相比,*P < 0.05,**P < 0.01,***P < 0.001。 图 7 各组主动脉炎症因子表达水平比较 |
5组小鼠的TC、HDL和LDL比较差异具有统计学意义(F=32.19~50.43,P < 0.001)。两两比较结果显示,APOE-/-小鼠的TC、HDL和LDL含量均高于A组小鼠(tLSD=8.529~12.540,P < 0.001),但各组APOE-/-小鼠中各指标含量并无明显差异(P>0.05)。见图 8。5组小鼠的胆固醇7α-羟化酶(CYP7A1)、ATP-结合盒转运子A1(ABCA1)和ATP-结合盒转运子G8(ABCG8)基因的表达水平比较差异具有统计学意义(F=7.975~37.120,P < 0.01)。两两比较结果显示,B组小鼠的CYP7A1、ABCA1和ABCG8基因的表达水平均低于A组(tLSD=3.185~3.622,P < 0.05);E组的CYP7A1、ABCA1和ABCG8表达水平高于C组、D组(tLSD=5.271~6.598,P < 0.05)。见图 9。
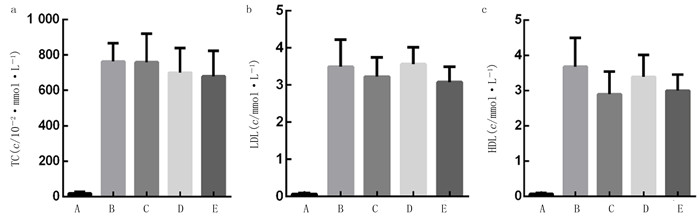 |
| a:血清中TC含量检测;b:血清中LDL含量检测;c:血清中HDL含量检测。A:空白对照组;B:实验对照组;C:LGG组;D:LA组;E:混合物组。 图 8 各组血脂含量比较 |
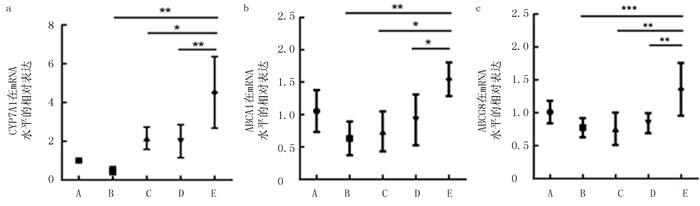 |
| a:小鼠肝脏中CYP7A1基因的表达水平;b:小鼠肝脏中ABCA1基因的表达水平;c:小鼠肝脏中ABCG8基因的表达水平。A:空白对照组;B:实验对照组;C:LGG组;D:LA组;E:混合物组。与E组相比,*P < 0.05,**P < 0.01,***P < 0.001。 图 9 各组肝脏中胆固醇转运分子表达水平的比较 |
近年来,心血管疾病死亡率呈上升趋势,是亟待解决的问题。动脉粥样硬化是心血管疾病的主要病理过程,是解决心血管疾病的重要切入点。研究发现,部分肠道菌群失调在很大程度上会促进或者抑制动脉粥样硬化的产生[21]。因此,找出哪些肠道菌群可以对动脉粥样硬化产生影响十分重要。为了确定益生菌灌胃后是否会被胃酸和胆盐在胃肠道中灭活,并影响益生菌在胃肠道中的定植,我们对LGG和LA进行了耐酸性和耐胆盐实验,结果显示两株菌具有良好的耐酸性与耐胆盐性。因此,我们进行了后续的动物实验。本研究发现,益生菌株联合干预组小鼠的主动脉主体内膜面与横截面的斑块面积明显减小,且效果优于单独益生菌干预组,提示益生菌联合干预可抑制动脉粥样斑块的形成。
TNF-α与IL-6是炎症反应过程中释放的细胞因子,是炎症的经典标志物。TNF-α与IL-6的高表达均会促进动脉粥样硬化的发生发展[22]。本研究结果显示,实验对照组的TNF-α与IL-6表达水平比空白对照组显著升高。益生菌干预后,这一情况得到抑制,且益生菌联合干预的抑制效果更明显。因此,我们推测益生菌可能通过抑制炎症反应来抑制动脉粥样硬化的发生发展。动脉粥样硬化的发生发展离不开脂质成分的累积[23]。本研究结果显示,APOE-/-小鼠血清中TC、HDL和LDL含量均显著高于空白对照组小鼠,但各组APOE-/-小鼠之间并无明显差异。推测这可能与菌株差异、灌胃时间较短或小鼠之间的个体差异相关。胆固醇代谢主要通过合成胆汁酸来实现[24],而CYP7A1是合成胆汁酸过程中的关键酶[25],ABCA1和ABCG8是促进胆固醇排出的基因[26-27]。本研究结果显示,对照组小鼠的CYP7A1、ABCA1和ABCG8基因的表达水平比空白对照组低,提示胆固醇代谢被抑制,胆固醇含量升高;经益生菌干预后,CYP7A1、ABCA1和ABCG8基因的表达水平显著升高,两菌株联合干预效果最明显。由此可见,益生菌联合干预可以显著抑制动脉粥样硬化的发生发展,并可能通过抑制炎症因子的表达以及增强胆固醇转运分子的表达而发挥抑制作用。
益生菌作为一种有益于人体健康的活菌,具有非常广泛的应用领域。在食品方面,在酸奶中添加保加利亚杆菌和乳酸菌能促进消化吸收;在疾病治疗方面,有治疗腹泻的双歧杆菌,治疗抑郁和焦虑的LGG等[28-30]。有研究显示,肠道菌群与动脉粥样硬化、2型糖尿病、结直肠癌等都有一定的关系[31-34],但在疾病的治疗方面尚无相关应用。因此,益生菌干预防治疾病需要继续探索和研究,这些成果为相关保健品的开发和临床应用提供了理论参考和支持,具有很大的市场应用潜力。
| [1] |
马丽媛, 王增武, 樊静, 等. 《中国心血管健康与疾病报告2021》要点解读[J]. 中国全科医学, 2022, 25(27): 3331-3346. DOI:10.12114/j.issn.1007-9572.2022.0506 |
| [2] |
LIU H H, CHEN X, HU X M, et al. Alterations in the gut microbiome and metabolism with coronary artery disease severity[J]. Microbiome, 2019, 7(1): 68. DOI:10.1186/s40168-019-0683-9 |
| [3] |
ZHU Y H, XIAN X M, WANG Z Z, et al. Research progress on the relationship between atherosclerosis and inflammation[J]. Biomolecules, 2018, 8(3): 80. DOI:10.3390/biom8030080 |
| [4] |
GEOVANINI G R, LIBBY P. Atherosclerosis and inflammation: overview and updates[J]. Clinical Science, 2018, 132(12): 1243-1252. DOI:10.1042/CS20180306 |
| [5] |
THIM T, HAGENSEN M K, BENTZON J F, et al. From vulnerable plaque to atherothrombosis[J]. Journal of Internal Medicine, 2008, 263(5): 506-516. DOI:10.1111/j.1365-2796.2008.01947.x |
| [6] |
ROWLAND I, GIBSON G, HEINKEN A, et al. Gut micro- biota functions: metabolism of nutrients and other food components[J]. European Journal of Nutrition, 2018, 57(1): 1-24. DOI:10.1007/s00394-017-1445-8 |
| [7] |
PISITHKUL T, SCHROEDER J W, TRUJILLO E A, et al. Metabolic remodeling during biofilm development of Bacillus subtilis[J]. mBio, 2019, 10(3): e00623-e00619. |
| [8] |
AVALL-JÄÄSKELÄINEN S, PALVA A. Lactobacillus surface layers and their applications[J]. FEMS Microbiology Reviews, 2005, 29(3): 511-529. |
| [9] |
ADAK A, KHAN M R. An insight into gut microbiota and its functionalities[J]. Cellular and Molecular Life Sciences, 2019, 76(3): 473-493. DOI:10.1007/s00018-018-2943-4 |
| [10] |
MINJ J, CHANDRA P, Paul C, et al. Bio-functional properties of probiotic Lactobacillus: current applications and research perspectives[J]. Critical Reviews in Food Science and Nutrition, 2021, 61(13): 2207-2224. DOI:10.1080/10408398.2020.1774496 |
| [11] |
SIVAMARUTHI B S, SUGANTHY N, KESIKA P, et al. The role of microbiome, dietary supplements, and probiotics in autism spectrum disorder[J]. International Journal of Environmental Research and Public Health, 2020, 17(8): 2647. DOI:10.3390/ijerph17082647 |
| [12] |
NI Y, YANG X, ZHENG L, et al. Lactobacillus and Bifidobacterium improves physiological function and cognitive ability in aged mice by the regulation of gut microbiota[J]. Molecular Nutrition & Food Research, 2019, 63(22): 1900603. |
| [13] |
CHEN L H, LIU W E, LI Y M, et al. Lactobacillus acidophilus ATCC 4356 attenuates the atherosclerotic progression through modulation of oxidative stress and inflammatory process[J]. International Immunopharmacology, 2013, 17(1): 108-115. DOI:10.1016/j.intimp.2013.05.018 |
| [14] |
HUANG Y, WANG J, QUAN G, et al. Lactobacillus acidophilus ATCC 4356 prevents atherosclerosis via inhibition of intestinal cholesterol absorption in apolipoprotein E-knockout mice[J]. Applied and environmental microbiology, 2014, 80(24): 7496-7504. DOI:10.1128/AEM.02926-14 |
| [15] |
ETTINGER G, BURTON J P, GLOOR G B, et al. Lactobacillus rhamnosus GR-1 attenuates induction of hypertrophy in cardiomyocytes but not through secreted protein MSP-1 (p75)[J]. PLoS One, 2017, 12(1): e0168622. DOI:10.1371/journal.pone.0168622 |
| [16] |
RIMBARA E, SUZUKI M, MATSUI H, et al. Isolation and characterization of Helicobacter suis from human stomach[J]. Proceedings of the National Academy of Sciences, 2021, 118(13): e2026337118. DOI:10.1073/pnas.2026337118 |
| [17] |
SCHICK P, SAGER M, WEGNER F, et al. Application of the GastroDuo as an in vitro dissolution tool to simulate the gastric emptying of the postprandial stomach[J]. Molecular Pharmaceutics, 2019, 16(11): 4651-4660. DOI:10.1021/acs.molpharmaceut.9b00799 |
| [18] |
KOH E, HWANG I Y, LEE H L, et al. Engineering probio- tics to inhibit Clostridioides difficile infection by dynamic regulation of intestinal metabolism[J]. Nature Communications, 2022, 13(1): 3834. DOI:10.1038/s41467-022-31334-z |
| [19] |
YOSHIDA N, EMOTO T, YAMASHITA T, et al. Bacteroides vulgatus and Bacteroides dorei reduce gut microbial lipopolysaccharide production and inhibit atherosclerosis[J]. Circulation, 2018, 138(22): 2486-2498. DOI:10.1161/CIRCULATIONAHA.118.033714 |
| [20] |
HONG Y F, KIM H, KIM H S, et al. Lactobacillus acidophilus K301 inhibits atherogenesis via induction of 24 (S), 25-epoxycholesterol-mediated ABCA1 and ABCG1 production and cholesterol efflux in macrophages[J]. PLoS One, 2016, 11(4): e0154302. DOI:10.1371/journal.pone.0154302 |
| [21] |
JIE Z Y, XIA H H, ZHONG S L, et al. The gut microbiome in atherosclerotic cardiovascular disease[J]. Nature Communications, 2017, 8(1): 845. DOI:10.1038/s41467-017-00900-1 |
| [22] |
PALMEFORS H, DUTTAROY S, RUNDQVIST B, et al. The effect of physical activity or exercise on key biomarkers in atherosclerosis: a systematic review[J]. Atherosclerosis, 2014, 235(1): 150-161. DOI:10.1016/j.atherosclerosis.2014.04.026 |
| [23] |
CARR S S, HOOPER A J, SULLIVAN D R, et al. Non-HDL-cholesterol and apolipoprotein B compared with LDL-cholesterol in atherosclerotic cardiovascular disease risk assessment[J]. Pathology, 2019, 51(2): 148-154. DOI:10.1016/j.pathol.2018.11.006 |
| [24] |
陈国良, 刘立伟, 谢爽, 等. 高密度脂蛋白胆固醇代谢及其对冠心病影响的研究进展[J]. 心血管病学进展, 2010, 31(3): 360-363. |
| [25] |
PULLINGER C R, ENG C, SALEN G, et al. Human cholesterol 7alpha-hydroxylase (CYP7A1) deficiency has a hypercholesterolemic phenotype[J]. The Journal of Clinical Investigation, 2002, 110(1): 109-117. DOI:10.1172/JCI0215387 |
| [26] |
PLŌSCH T, KOK T, BLOKS V W, et al. Increased hepatobiliary and fecal cholesterol excretion upon activation of the li- ver X receptor is independent of ABCA1[J]. The Journal of Biological Chemistry, 2002, 277(37): 33870-33877. DOI:10.1074/jbc.M206522200 |
| [27] |
REPA J J, BERGE K E, POMAJZL C, et al. Regulation of ATP-binding cassette sterol transporters ABCG5 and ABCG8 by the liver X receptors alpha and beta[J]. The Journal of Biological Chemistry, 2002, 277(21): 18793-18800. DOI:10.1074/jbc.M109927200 |
| [28] |
MOLUDI J, KHEDMATGOZAR H, NACHVAK S M, et al. The effects of co-administration of probiotics and prebiotics on chronic inflammation, and depression symptoms in patients with coronary artery diseases: a randomized clinical trial[J]. Nutritional Neuroscience, 2022, 25(8): 1659-1668. DOI:10.1080/1028415X.2021.1889451 |
| [29] |
SMITH T J, RIGASSIO-RADLER D, DENMARK R, et al. Effect of Lactobacillus rhamnosus LGG® and Bifidobacterium animalis ssp. lactis BB-12® on health-related quality of life in college students affected by upper respiratory infections[J]. The British Journal of Nutrition, 2013, 109(11): 1999-2007. DOI:10.1017/S0007114512004138 |
| [30] |
GAGNON E, MITCHELL P L, MANIKPURAGE H D, et al. Impact of the gut microbiota and associated metabolites on cardiometabolic traits, chronic diseases and human longevity: a Mendelian randomization study[J]. Journal of Translational Medicine, 2023, 21(1): 60. DOI:10.1186/s12967-022-03799-5 |
| [31] |
HORIE M, MIURA T, HIRAKATA S, et al. Comparative analysis of the intestinal flora in type 2 diabetes and nondiabetic mice[J]. Experimental Animals, 2017, 66(4): 405-416. DOI:10.1538/expanim.17-0021 |
| [32] |
MA Q T, LI Y Q, LI P F, et al. Research progress in the relationship between type 2 diabetes mellitus and intestinal flora[J]. Biomedecine & Pharmacotherapie, 2019, 117: 109138. |
| [33] |
SI H F, YANG Q, HU H, et al. Colorectal cancer occurrence and treatment based on changes in intestinal flora[J]. Seminars in Cancer Biology, 2021, 70: 3-10. DOI:10.1016/j.semcancer.2020.05.004 |
| [34] |
ZHOU X Y, CHEN C X, ZHONG Y N, et al. Effect and mechanism of vitamin D on the development of colorectal cancer based on intestinal flora disorder[J]. Journal of Gastroenterology and Hepatology, 2020, 35(6): 1023-1031. DOI:10.1111/jgh.14949 |
 2024, Vol. 60
2024, Vol. 60

