2. 青岛市胸科医院放射科, 山东 青岛 266043;
3. 青岛市胸科医院外科, 山东 青岛 266043
自2019年12月, 我国武汉地区及世界多个国家和地区暴发了由新型冠状病毒(SARS-CoV-2)感染引起的新型冠状病毒肺炎(COVID-19)。此病传染性极高,至今未发现其防治特效药物及有效疫苗。本研究对我院收治的40例COVID-19确诊病人的临床资料进行分析,旨在为其诊治提供依据。
1 资料与方法 1.1 一般资料2020年1月26日-4月20日,在我院住院治疗COVID-19确诊病人40例,均符合《新型冠状病毒肺炎诊疗方案》(试行第3~7版)诊断标准[1-5]。男15例,女25例;年龄为5~78岁,平均(45.55±15.75)岁。出院标准[5]:①体温恢复正常3 d以上,呼吸道症状明显好转;②肺部影像学显示炎症明显吸收;③连续2次呼吸道病原核酸检测阴性,采样时间间隔至少24 h。治疗过程中2例普通型病人转为重症型,经治疗所有病人均治愈出院。本研究经医院医学伦理委员会批准,病人均知情同意。
1.2 调查方法回顾该组病人的临床表现、外周血液检验结果、发病初期的肺部CT影像学特征及疾病转归,分析发病初期的肺部影像学特征、临床表现、外周血液检验结果及其与疾病转归的相关性。
1.3 实验室检查病人入院后第2天采集空腹静脉血,进行外周血白细胞计数、淋巴细胞计数、C反应蛋白(CRP)、肌酐、红细胞沉降率、咽拭子SARS-CoV-2核酸等检查。出院前两次咽拭子SARS-CoV-2核酸检查阴性,其中发病与第一次咽拭子核酸检测阴性间隔时间为SARS-CoV-2核酸转阴时间。
1.4 影像学检查所有病人均进行CT扫描。设备采用飞利浦16排螺旋CT;病人均采取仰卧位, 扫描范围从胸廓入口至双侧肋弓下缘; 扫描参数为:120 kV, 100~200 mA。根据疾病发展的影像学特点,将肺部影像学表现分为4期:1期无明显肺部阴影;2期仅存在多发小斑片影及间质改变,肺外带明显;3期存在双肺多发磨玻璃影、浸润影,无肺实变;4期在3期基础上出现肺实变。多发:指病灶分布在两个以上肺段(含两个肺段)。每例病人肺部影像分期以其肺部病变影像进展的最高峰判定[5]。各期典型CT影像特征及转归见图 1。
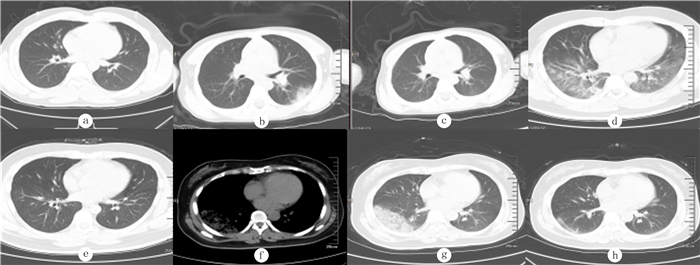 |
| a:1期,无明显肺部阴影;b:2期,仅存在多发小斑片状影及间质改变,肺外带明显;d:3期,存在双肺多发磨玻璃影、浸润影,无肺实变;f、g:4期,存在肺实变;c、e、h:治疗后影像,病灶明显吸收。 图 1 COVID-19病人各期治疗前后胸部CT影像 |
采用SPSS 17.0软件进行统计学分析。计数资料以频数表示,组间比较采用卡方检验;正态分布计量资料以x±s表示,组间数据比较采用独立样本t检验;非正态分布计量资料以中位数和四分位数间距(M(P25~P75))表示,组间数据比较采用H检验。相关性分析采用Spearman相关分析。以P < 0.05为差异有统计学意义。
2 结果 2.1 临床特征及影像学表现本文40例病人中,37例(92.5%)有症状,17例(42.5%)伴有基础疾病,31例(77.5%)出现发热。肺部影像学特征分期情况:1期3例,2期22例,3期10例,4期5例。病人的肺部影像学表现越重,越容易产生发热症状(χ2=7.876,P=0.030)、CRP越高(H=12.562,P=0.006)、发热时间越长(H=8.548, P=0.036);肺部影像学表现与年龄(H=4.218, P=0.239)、白细胞计数(H=2.960, P=0.398)、淋巴细胞计数(H=4.079, P=0.253)、红细胞沉降率(H=3.404, P=0.333)、SARS-CoV-2核酸转阴时间(H=2.206, P=0.531)、肌酐(H=6.151, P=0.105)、性别(χ2=3.495, P=0.314)、有无症状(χ2=1.796, P=0.766)及是否有基础疾病(χ2=3.185, P=0.395)等无关。最终40例病人肺部病灶均吸收。见表 1。
| 表 1 COVID-19病人肺部影像学特征与相关因素的关系(M(P25~P75)) |
|
|
本文40例病人中,外周血白细胞平均计数为(4.67±1.47)×109/L,其中15例(37.5%)病人减少,25例(63.5%)正常;外周血淋巴细胞平均计数为(1.55±0.69)×109/L,其中2例(5.0%)病人减少,38例(95.0%)正常;红细胞沉降率为(47.72±26.80)mm/ 1 h,其中32例(80.0%)病人增快,8例(20.0%)正常;血清肌酐平均(49.98±18.69)μmol/L,其中22例(55.0%)病人降低,18例(45.0%)正常;CRP(22.69±27.54)mg/L,其中20例(50.0%)病人升高,20例(50.0%)正常;31例(77.5%)病人出现发热,发热时间(4.85±4.34)d;SARS-CoV-2核酸转阴时间(21.92±6.58)d;SARS-CoV-2抗体IgG产生时间(15.07±6.17)d。
2.3 咽拭子SARS-CoV-2核酸转阴时间影响因素咽拭子SARS-CoV-2核酸转阴时间与CRP、年龄、外周血白细胞及淋巴细胞计数、红细胞沉降率、发热时间、肌酐、性别、有无症状、是否发热及有基础疾病等均无关(r=-1.237~0.914,P>0.05)。
3 讨论SARS-CoV-2是第7种人类冠状病毒,属于β冠状病毒,但与SARS-CoV和MERS-CoV等有明显的区别,在人与人之间存在强大的传染性[5-6]。CHEN等[7]研究结果显示,在国内有武汉旅居史的COVID-19病人只占病人总数的49%。全球多国出现疫情暴发且蔓延迅速,证明此病在人与人之间传染性相当强, 但至今为止病毒源头仍未明确。
SARS-CoV-2是一种具有包膜的病毒,其包膜与宿主细胞膜融合后可在宿主体内大量繁殖[8]。宿主暴露后,SARS-CoV-2通过呼吸道进入宿主的体内[9],与具有表达血管紧张素转化酶2(ACE2)受体的细胞结合,进入细胞内部进行复制[10]。在ACE2的作用下,病毒S蛋白经系列裂解与重构,最终病毒紧密融合于细胞膜[11]。人类的肺、心脏中存在大量ACE2受体,SARS-CoV-2感染后,较易出现相关症状。有研究结果显示,部分COVID-19病人可出现嗅觉及味觉减退或丧失的表现[12]。另外,本研究中有55.00%的病人肌酐下降。分析原因可能为病毒S蛋白与鼻黏膜、脑神经及肾脏的ACE2受体结合导致上述症状的产生。
HEITZMAN等[13]提出将肺分为中央的肺髓质和周围的肺皮质。肺皮质内的肺小叶相对更大, 呈弧形或扇形排列。这些结构构成了COVID-19影像学特征的理论基础。COVID-19疾病早期呈现多发小斑片影及间质改变, 以肺外带明显, 进而发展为双肺多发磨玻璃影、浸润影[5]。多项研究指出,COVID-19病人双侧肺受累的概率及肺部影像学特点与尸检病理报告结果一致[5, 14]。本研究COVID-19病人肺部影像学表现与上述研究结果一致。
本研究中病人肺部影像特征与性别、年龄、基础疾病均无明显相关性。CHEN等[7]研究结果显示,男性COVID-19病人病变程度明显较女性病人重,分析其原因可能与女性的X基因及性激素有关。本文研究结果与其不一致,需要大样本循证研究进一步证实。本研究结果显示,COVID-19肺部病变越重,发热时间越长,治疗过程中向重症发展的可能性越大。目前研究已证实,重症COVID-19病人多在发病1周后出现呼吸困难和(或)低氧血症,严重者可快速进展为急性呼吸窘迫综合征、脓毒症性休克等。对于COVID-19病人在肺部病变处于上升期时,建议每3 d复查一次胸部CT。本研究40例病人中有5例为重症,其中2例为入院后由普通型转为重症,提示在经积极抗病毒和中医治疗后,即使病人指氧饱和度没有明显下降,发热超过5 d也应尽早复查胸部CT,以明确病情变化。
本研究病人均在发病后获得SARS-CoV-2抗体IgG,抗体的产生时间均在发病后1周以上,这与机体的免疫应答时间有关。本文研究未发现咽拭子SARS-CoV-2核酸转阴时间与病情有相关性,可能与本研究病人以轻型和普通型为主有关。这与王素娜等[14]报道的咽拭子转阴时间与病变程度、年龄及基础疾病呈正相关不一致,与张瑞珍等[15]报道一致。本研究病人中,有3例为无症状感染病人,咽拭子SARS-CoV-2核酸转阴时间偏长,分别为18、30、38 d,其原因可能为无症状感染者所感染的SARS-CoV-2更易逃脱宿主的免疫应答,不产生相应症状,从而导致宿主免疫系统对病毒的清除反而较难。但因本研究无症状病人较少,难以形成有效对照,需要大样本资料进行循证研究。
综上所述,COVID-19病人的肺部病变范围越广泛,导致发热可能性越大,而且病变越重发热时间越长。IgG抗体的形成是必然结果,但时间一般在感染后1周以上;咽拭子SARS-CoV-2核酸转阴时间与病情无相关性。在流行病学的基础上,关注发热、病毒核酸及SARS-CoV-2抗体检测的同时,可行CRP、红细胞沉降率、肌酐等检测作为无症状感染者的参考指标,以避免漏诊。
| [1] |
国家卫生健康委员会, 国家中医药管理局办公室. 新型冠状病毒感染的肺炎诊疗方案(试行第3版)[EB/OL]. (2020-01-22)[2020-6-13]. http://www.nhc.gov.cn/xcs/zhengcwj/202001/f492c9153ea9437bb587ce2ffcbee1fa/files/39e7578d85964dbe8-1117736dd789d8f.pdf.
|
| [2] |
国家卫生健康委员会. 新型冠状病毒肺炎诊疗方案(试行第4版)[EB/OL]. (2020-01-27)[2020-06-13]. http://www.nhc.gov.cn/xcs/zhengcwj/202001/4294563ed35b43209b31739bd-0785e67.shtml.
|
| [3] |
国家卫生健康委员会. 新型冠状病毒肺炎诊疗方案(试行第5版修正版)[EB/OL]. (2020-02-08)[2020-06-13]. http://www.nhc.gov.cn/xcs/zhengcwj/202002/d4b895337e19445-f8d728fcaf1e3e13a.shtml.
|
| [4] |
国家卫生健康委员会. 关于印发新型冠状病毒肺炎诊疗方案(试行第6版)[EB/OL]. (2020-02-18)[2020-06-13]. http://www.nhc.gov.cn/yzygj/s7653p/202002/8334a8326dd94d32-9df351d7da8aefc2/files/b218cfeb1bc54639af227f922bf6b817.pdf.
|
| [5] |
国家卫生健康委员会. 新型冠状病毒肺炎诊疗方案(试行第7版)[EB/OL]. (2020-03-03)[2020-06-13]. http://www.nhc.gov.cn/yzygj/s7653p/202003/46c9294a7dfe4cef80dc7f5912eb-1989/files/ce3e6945832a438eaae415350a8ce964.pdf.
|
| [6] |
CHAN J F, KOK K H, ZHU Z, et al. Genomic characterization of the 2019 novel human-pathogenic coronavirus isolated from a patient with atypical pneumonia after visiting Wuhan[J]. Emerging Microbes & Infections, 2020, 9(1): 221-236. |
| [7] |
CHEN N S, ZHOU M, DONG X, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study[J]. Lancet (London, England), 2020, 395(10223): 507-513. DOI:10.1016/S0140-6736(20)30211-7 |
| [8] |
WANG H L, YANG P, LIU K T, et al. SARS coronavirus entry into host cells through a novel clathrin- and caveolae-independent endocytic pathway[J]. Cell Research, 2008, 18(2): 290-301. DOI:10.1038/cr.2008.15 |
| [9] |
GRALINSKI L E, MENACHERY V D. Return of the Coronavirus: 2019-nCoV[J]. Viruses, 2020, 12(2): 135. DOI:10.3390/v12020135 |
| [10] |
ZHOU P, YANG X L, WANG X G, et al. Addendum: a pneumonia outbreak associated with a new coronavirus of probable bat origin[J]. Nature, 2020, 588(7836): E6. DOI:10.1038/s41586-020-2951-z |
| [11] |
WRAPP D, WANG N S, CORBETT K S, et al. Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation[J]. Science, 2020, 367(6483): 1260-1263. DOI:10.1126/science.abb2507 |
| [12] |
GAUTIER J F, RAVUSSIN Y. A new symptom of COVID-19: loss of taste and smell[J/OL]. ReaserchGate, 2020, 28(5). doi: 10.1002/oby.22809.
|
| [13] |
HEITZMAN E R, MARKARIAN B, BERGER L, et al. The secondary pulmonary lobule: a practical concept for interpretation of chest radiographs.l.Roentgen anatomy of the normal secondary pulmonary lobule[J]. Radiology, 1969, 93(3): 507-512. DOI:10.1148/93.3.507 |
| [14] |
王素娜, 姚娜, 汪春付, 等. 新型冠状病毒肺炎39例临床特征分析[J]. 陕西医学杂志, 2020, 49(6): 643-647, 652. DOI:10.3969/j.issn.1000-7377.2020.06.001 |
| [15] |
张瑞珍, 吴茱萸, 陈小华, 等. 新型冠状病毒肺炎患者治疗后不同核酸转阴时间的临床特征比较[J]. 微生物学免疫学进展, 2020, 48(2): 48-52. |
 2021, Vol. 57
2021, Vol. 57

