斑秃是一种非瘢痕性、炎症性脱发,常见的临床表现为头部出现边界清晰的圆形或椭圆形斑状脱发。斑秃的致病机制是T淋巴细胞介导的、以毛囊为靶器官的器官特异性自身免疫性疾病,并与神经精神因素、内分泌及遗传因素相关。国内的一些研究调查了斑秃与甲状腺自身免疫之间的联系[1-6],但是,大多数研究样本量相对较小,所获得的结果不能证实斑秃与甲状腺自身免疫之间是否存在关联。本研究检索了1974年1月1日—2016年4月20日期间国内外发表的斑秃与甲状腺自身免疫的相关性研究文献,应用Meta方法分析判断斑秃与甲状腺自身免疫的相关性,以期为斑秃防治提供依据。
1 资料与方法 1.1 文献及其来源① 在万方数据库、中国生物医学数据库(CBM)、中国知网(CNKI)中,以“斑秃”和“甲状腺”为检索词,对题目、摘要、关键词进行检索;②在Pubmed、Embase、Cochrane数据库中,以“alopecia areata”或“alopecia circumscripta”、“thyroidgland”或“thyroid”为检索词,对题目、摘要、关键词进行检索。起止时间为1974年1月1日—2016年4月20日。
1.2 文献纳入标准与质量控制纳入标准:①为斑秃与甲状腺自身免疫的相关性研究;②排除其他系统性疾病及自身免疫性疾病;③必须包括测量甲状腺自身抗体和(或)甲状腺功能的实验室检查;④必须已经以英文或中文全文发表;⑤有健康对照组,甲状腺疾病处于亚临床或临床状态。排除标准:①样本量少于20例的研究;②仅有定量数据而无患病率的文献;③重复多次发表的文献、数据不完整的文献、质量方法学低的文献;④综述、讲座、评论类以及其他非科研类文献。质量控制:根据纳入和剔除标准仔细阅读全文后确定文献是否入选。质量评价由两名研究者独立进行,意见不同时由第3名研究者评判决定。
1.3 数据提取从每项研究中提取文献的第一作者、发表年份、国家、斑秃组人数、健康对照组人数、性别、斑秃类型、成人或儿童、平均年龄、有或没有实验室检查、甲状腺功能检查结果。根据实验室检查结果将研究对象分为3组:甲状腺功能异常组、自身免疫性甲状腺疾病(AITD)组、甲状腺自身抗体阳性组。甲状腺功能异常组为甲状腺功能异常,伴或不伴有甲状腺自身抗体阳性;AITD组为甲状腺功能异常且有甲状腺自身抗体阳性者;甲状腺自身抗体阳性组为任何一种甲状腺自身抗体升高者。
1.4 Meta分析方法采用RevMan 5.3软件、Stata软件进行Meta分析。①效应量选择:运用二分类变量,计算各项研究文献中斑秃组与健康对照组甲状腺功能异常、AITD、甲状腺自身抗体阳性人数的比值比(OR),用95%可信区间(CI)表示。②异质性检验:应用χ2检验对文献数据进行异质性检验,如果文献数据间不存在异质性(P>0.05),则选择固定效应模型进行下一步的统计分析;如果文献数据间存在异质性(P<0.05),则选择随机效应模型进行下一步的统计分析。分别计算各项研究文献中斑秃病例组和健康对照组AITD及甲状腺自身抗体阳性OR值及其95%CI、Z统计量及其概率值。P<0.05为差异有统计学意义。③发表性偏倚分析:用漏斗图进行分析,如果漏斗图显示结果基本对称,则说明可能不存在发表性偏倚。用Stata软件进行Begg’s和Egger检测,若两者P>0.05,说明结果不具有统计学意义,不存在发表偏倚;否则相反。
2 结果 2.1 文献基本情况文献筛选流程及结果见图 1。入选文献共有29篇,其中以中文发表文献6篇,以英文发表文献23篇,包括中国台湾1篇、美国6篇、英国1篇、西班牙1篇、荷兰1篇、保加利亚1篇、土耳其1篇、沙特阿拉伯1篇、伊朗1篇、科威特1篇、澳大利亚1篇、日本2篇、印度2篇、泰国1篇、蒙古2篇[1-29]。累计斑秃病人12 571人,健康对照组790 182人。见表 1。
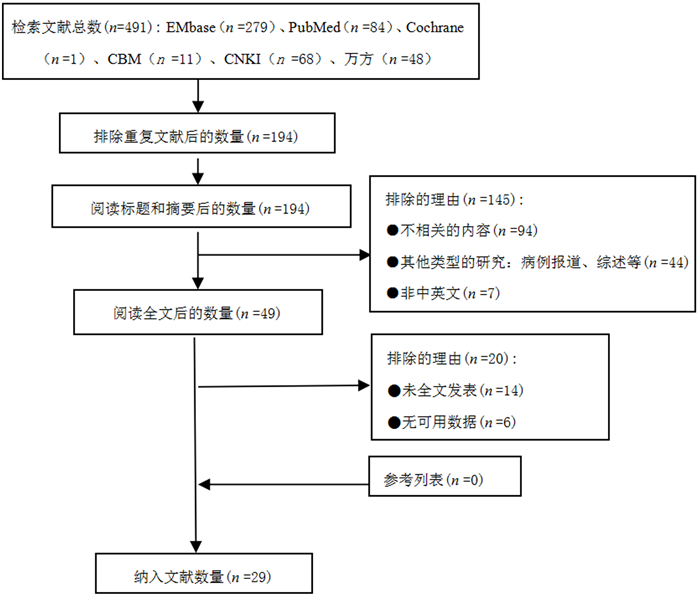 |
| 图 1 搜索策略和文献筛选流程图 |
| 表 1 斑秃与甲状腺自身免疫相关性研究文献的基本情况(例) |
|
|
纳入的29篇文献中,斑秃组病人12 571人,其中AITD、甲状腺自身抗体和甲状腺功能异常的阳性率分别为0.102%、0.117%和0.093%;健康对照组790 182人,其中AITD、甲状腺自身抗体和甲状腺功能异常的阳性率分别为0.016%、0.084%和0.040%。斑秃组与健康对照组相比较,甲状腺自身抗体阳性率差异有统计学意义(U=19.000,P<0.01),AITD和甲状腺功能异常阳性率差异无统计学意义(P>0.05)。纳入的文献中有12篇为病例对照研究,Meta分析显示,AITD组总体OR=3.48(Z=4.37, P<0.01, 95%CI=1.99~6.10), 异质性检验χ2=2.22, df=2(P=0.33), I2=10%,表示各文献之间同质性较好,适合进行固定效应模型Meta分析(图 2);甲状腺自身抗体阳性组总体OR=5.28(Z=11.85, P<0.01, 95%CI=4.01~6.95);异质性检验χ2=10.70,df=8(P=0.22),I2=25%,表示各文献间的同质性较好,适合固定效应模型Meta分析(图 3);甲状腺功能异常组总体OR=3.92(Z=2.42, P=0.02, 95%CI=1.30-11.86), 异质性检验χ2=14.68, df=2(P=0.000 6), I2=86%,表示各文献之间异质性过高,但因文献数量过少,仅为3篇,暂不能明确异质性来源。故本文放弃斑秃与甲状腺功能异常相关性的Meta分析。
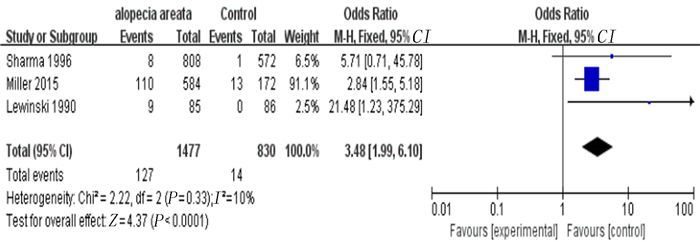 |
| 图 2 斑秃与AITD相关性Meta分析的森林图(固定效应模型) |
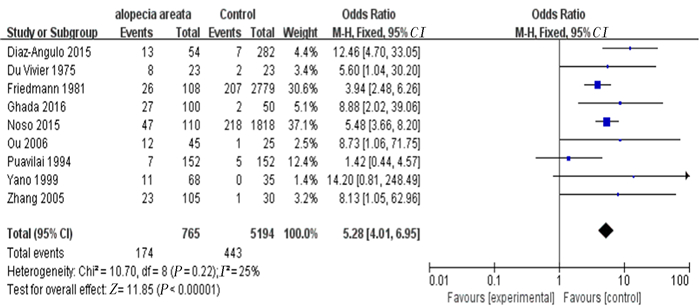 |
| 图 3 斑秃与甲状腺自身抗体相关性Meta分析的森林图(固定效应模型) |
应用Meta回归分析方法检测甲状腺自身抗体阳性组异质性来源,结果显示各文献结果之间的差异与斑秃组人数有关(P=0.047)。见表 2。本文因AITD组纳入文献数量较少,故未行Meta回归分析。
| 表 2 斑秃与甲状腺自身抗体相关性的Meta回归分析 |
|
|
甲状腺自身抗体阳性组以OR值的对数和对数的标准误分别作为纵坐标和横坐标绘制漏斗图,各研究在总体OR值两侧分布基本对称(图 4);共纳入9篇文献,经Egger检验不存在发表偏倚(P=0.481)。因AITD组纳入文献数量较少,故未行发表偏倚检测。
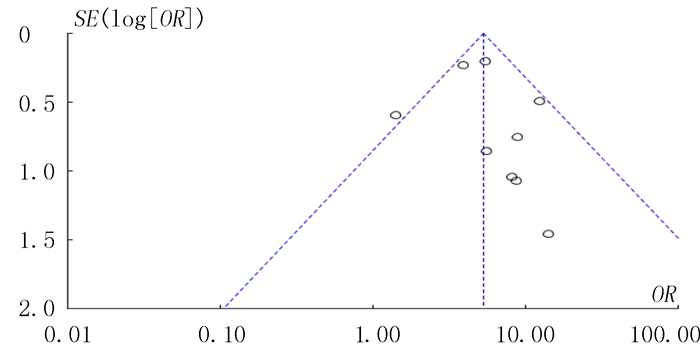 |
| 图 4 斑秃与甲状腺自身抗体相关性Meta分析的漏斗图(固定效应模型) |
斑秃的病因尚不完全清楚,可能与遗传、自身免疫、环境因素等有关。近年来有研究显示,自身免疫在斑秃的发病中起主要作用[30-31],而AITD是最常见的自身免疫性疾病,因此本文对斑秃与甲状腺自身免疫之间的相关性进行了研究。
本文共纳入29篇文献,其中12篇为病例对照研究,获取的数据共分为3组:甲状腺功能异常组、AITD组和甲状腺自身抗体阳性组,其中甲状腺功能异常组因异质性过大、文献数量过少而放弃分析。结果显示,斑秃组甲状腺自身抗体阳性率高于健康对照组,差异有统计学意义,提示斑秃与甲状腺自身免疫具有相关性。
有研究认为发表偏倚会显著影响Meta分析的效力[32]。本文研究虽然甲状腺自身抗体阳性组纳入文献的数量较少,仅为9篇,但无论是漏斗图还是Egger统计学检验,结果均表明纳入的9篇文献不存在显著性发表偏倚。Meta回归分析结果显示,斑秃组样本量对斑秃与甲状腺自身抗体相关性的影响具有显著性。出现这种结果的原因可能是:纳入文献中斑秃组样本量最大者仅有152例,而人群中甲状腺自身抗体的阳性率较低,想要获得比较可信的结果,需要有更大的样本量。因此,应谨慎理解本文中Meta分析的相关性结果。
目前有研究发现,与斑秃并发的甲状腺疾病中甲状腺功能减退最为常见[1]。甲状腺功能减退可影响毛发的质地并引起毛发脱落,可能由于甲状腺功能减退引起机体代谢降低,处于静止期的毛发增加,转化为生长期的速度减慢甚至转化失败,从而引起脱发[33]。由于不是所有的甲状腺功能减退病人都有脱发,因此,甲状腺激素对毛发的影响可能还受局部因素和其他激素的影响。部分斑秃病人检测到了甲状腺自身抗体,尽管当时没有明显甲状腺疾病,但将来发生甲状腺功能不全的风险将会增加[15]。
综上所述,斑秃与甲状腺自身免疫具有相关性,对斑秃病人筛查甲状腺自身抗体具有必要性。但本研究具有局限性,一是纳入的研究样本量较小,影响了结果的可靠性;二是缺乏职业、种族、饮食、精神等潜在混杂影响因素信息,对本次分析结果可能会产生一定影响。因此,斑秃与甲状腺自身免疫的相关性有待于更加深入的研究,以找到斑秃的确切致病机制以及根治方法。
| [1] |
杨竹生, 杨秀敏, 金星姬, 等. 成人斑秃与甲状腺自身免疫的关系分析[J]. 中华皮肤科杂志, 2015, 48(10): 697-699. DOI:10.3760/cma.j.issn.0412-4030.2015.10.008 |
| [2] |
丁俐元.斑秃患者自身抗体检测及临床分析[D].广州: 广州中医药大学, 2014. http://d.wanfangdata.com.cn/Thesis_Y2623456.aspx
|
| [3] |
欧阳莹.儿童斑秃免疫学发病机制的初步探讨[D].重庆: 重庆医科大学, 2006. http://med.wanfangdata.com.cn/Paper/Detail/DegreePaper_Y956035
|
| [4] |
陈明, 潘红梅. 50例婴幼儿斑秃相关因素分析[J]. 中国麻风皮肤病杂志, 2006, 22(6): 481-482. DOI:10.3969/j.issn.1009-1157.2006.06.017 |
| [5] |
张杏莲, 刘强. 儿童斑秃患者甲状腺抗体及甲状腺功能的研究[J]. 山西医药杂志, 2005, 34(4): 315-316. DOI:10.3969/j.issn.0253-9926.2005.04.025 |
| [6] |
罗敏, 黄进华, 廖朝晖, 等. 斑秃118例临床分析[J]. 中华医学美学美容杂志, 2004, 10(6): 342-345. DOI:10.3760/cma.j.issn.1671-0290.2004.06.008 |
| [7] |
BIN SAIF G A. Severe subtype of alopecia areata is highly associated with thyroid autoimmunity[J]. Saudi Medical Journal, 2016, 37(6): 656-661. DOI:10.15537/smj.2016.6.13777 |
| [8] |
KURTIPEK G S, CIHAN F G, DEMIRBAS S E, et al. The frequency of autoimmune thyroid disease in alopecia areata and vitiligo patients[J]. BioMed Research International, 2015, 2015: 1-4. |
| [9] |
NOSO S, PARK C, BABAYA N, et al. Organ specificity in autoimmune diseases: thyroid and islet autoimmunity in alopecia areata[J]. The Journal of Clinical Endocrinology & Metabolism, 2015, 100(5): 1976-1983. |
| [10] |
MILLER R, CONIC R Z, BERGFELD W, et al. Prevalence of comorbid conditions and sun-induced skin cancers in patients with alopecia areata[J]. The Journal of Investigative Dermatology. Symposium Proceedings/the Society for Investigative Dermatology, Inc. and European Society for Dermatological Research, 2015, 17(2): 61-62. DOI:10.1038/jidsymp.2015.44 |
| [11] |
LYAKHOVITSKY A, SHEMER A, AMICHAI B. Increased prevalence of thyroid disorders in patients with new onset alopecia areata[J]. Australasian Journal of Dermatology, 2015, 56(2): 103-106. DOI:10.1111/ajd.12178 |
| [12] |
DIAZ-ANGULO S, LOPEZ-HOYOS M, MUNOZ-CACHO P, et al. High prevalence of thyroid autoimmunity in patients with alopecia areata and vitiligo: a controlled study[J]. Australasian Journal of Dermatology, 2015, 56(2): 142-143. |
| [13] |
LUNDIN M, CHAWA S, SACHDEV A, et al. Gender differences in alopecia areata[J]. Journal of Drugs in Dermatology: JDD, 2014, 13(4): 409-413. |
| [14] |
HUANG K P, MULLANGI S, GUO Y, et al. Autoimmune, atopic, and mental health comorbid conditions associated with alopecia areata in the United States[J]. JAMA Dermatology (Chicago, Ill.), 2013, 149(7): 789-794. DOI:10.1001/jamadermatol.2013.3049 |
| [15] |
BAARS M P, GREEBE R J, POP V J. High prevalence of thyroid peroxidase antibodies in patients with alopecia areata[J]. Journal of the European Academy of Dermatology and Venereology: JEADV, 2013, 27(1): e137-e139. DOI:10.1111/j.1468-3083.2011.04420.x |
| [16] |
CHU S Y, CHEN Y J, TSENG W C, et al. Comorbidity profiles among patients with alopecia areata: the importance of onset age, a nationwide population-based study[J]. Journal of the American Academy of Dermatology, 2011, 65(5): 949-956. DOI:10.1016/j.jaad.2010.08.032 |
| [17] |
GOH C, FINKEL M, CHRISTOS P J, et al. Profile of 513 patients with alopecia areata: associations of disease subtypes with atopy, autoimmune disease and positive family history[J]. Journal of the European Academy of Dermatology and Venereology, 2006, 20(9): 1055-1060. DOI:10.1111/j.1468-3083.2006.01676.x |
| [18] |
SEYRAFI H, AKHIANI M, ABBASI H, et al. Evaluation of the profile of alopecia areata and the prevalence of thyroid function test abnormalities and serum autoantibodies in Iranian patients[J]. BMC Dermatology, 2005, 5(1): 1-5. DOI:10.1186/1471-5945-5-1 |
| [19] |
KURTEV A, ILIEV E. Thyroid autoimmunity in children and adolescents with alopecia areata[J]. International Journal of Dermatology, 2005, 44(6): 457-461. DOI:10.1111/j.1365-4632.2005.01971.x |
| [20] |
NANDA A, ALSALEH Q A, FOWZIA AL-HASAWI, et al. Thyroid function, autoantibodies, and hla tissue typing in children with alopecia areata[J]. Pediatric Dermatology, 2002, 19(6): 6. |
| [21] |
YANO S, IHN H, NAKAMURA K, et al. Antinuclear and antithyroid antibodies in 68 Japanese patients with alopecia areata[J]. Dermatology, 1999, 199(2): 191. DOI:10.1159/000018241 |
| [22] |
SHARMA V K, SIALY R, KUMAR B, et al. Evaluation of thyroid function in North Indians with alopecia areata:response to intravenous injection of 100 micrograms thyrotropin releasing hormone(TRH)[J]. Journal of Dermatology, 1999, 26(6): 339-342. DOI:10.1111/j.1346-8138.1999.tb03484.x |
| [23] |
SHARMA V K, GOUTAM D, BHUSHAN K. Profile of alopecia areata in Northern India[J]. International Journal of Dermatology, 1996, 35(1): 22-27. |
| [24] |
PUAVILAI S, PUAVILAI G, CHARUWICHITRATANA S, et al. Prevalence of thyroid-diseases in patients with alopecia-areata[J]. International Journal of Dermatology, 1994, 33(9): 632-633. DOI:10.1111/j.1365-4362.1994.tb02921.x |
| [25] |
LEWI |
| [26] |
KORKIJ W, SOLTANI K, SIMJEE S, et al. Tissue-specific autoantibodies and autoimmune disorders in vitiligo and alopecia areata:a retrospective study[J]. Journal of Cutaneous Pathology, 1984, 11(6): 522-530. DOI:10.1111/j.1600-0560.1984.tb00413.x |
| [27] |
FRIEDMANN P S. Alopecia areata auto-immunity[J]. British Journal of Dermatology, 1981, 105(2): 153-157. DOI:10.1111/j.1365-2133.1981.tb01200.x |
| [28] |
VIVIER A D, MUNRO D D. Alopecia areata, autoimmunity, and Down's syndrome[J]. BMJ, 1975, 1(5951): 191-192. DOI:10.1136/bmj.1.5951.191 |
| [29] |
VIVIER A D, MUNRO D D. Alopecia areata and mongolism[J]. Proceedings of the Royal Society of Medicine, 1974, 67(7): 596-596. DOI:10.1177/003591577406700709 |
| [30] |
ISLAM N, LEUNG P S, HUNTLEY A C, et al. The autoimmune basis of alopecia areata: a comprehensive review[J]. Autoimmunity Reviews, 2015, 14(2): 81-89. DOI:10.1016/j.autrev.2014.10.014 |
| [31] |
杨竹生, 林麟. 自身反应性T细胞与斑秃[J]. 国际皮肤性病学杂志, 2006, 32(6): 362-364. DOI:10.3760/cma.j.issn.1673-4173.2006.06.010 |
| [32] |
SUTTON J A. Empirical assessment of effect of publication bias on meta-analyses[J]. BMJ, 2000, 320(7249): 1574-1577. DOI:10.1136/bmj.320.7249.1574 |
| [33] |
THOMAS E A, KADYAN R S. Alopecia areata and autoimmunity:a clinical study[J]. Indian Journal of Dermatology, 2008, 53(2): 70-74. DOI:10.4103/0019-5154.41650 |
 2019, Vol. 55
2019, Vol. 55


 SKI
SKI